对于下列氧化还原反应,请按要求填空。
(1)Cu + 4HNO3(浓) === Cu(NO3)2 + 2NO2↑ + 2H2O
①用单线桥法标出电子转移的方向和数目_____________。
②氧化剂____________氧化产物_____________ ③离子方程式:_________________。
(2)2H2S + SO2 === 3S↓ + 2H2O
①用双线桥法标出电子转移的方向和数目_______________。
②若氧化产物比还原产物多1.6g,则反应中电子转移的个数为________________ 。
答案 : (1)①
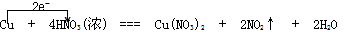
②HNO3 ;Cu(NO3)2
③Cu+4H++2NO3-===Cu2+ +2NO2↑+2H2O
(2)①
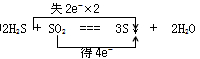
②1.204×1023
KClO3和浓盐酸在一定温度下反应会生成黄绿色的 易爆物二氧化氯。其变化可表示为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(用双线桥法表示)___________。
(2)浓盐酸在反应中显示出来的性质是____(填序号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)若产生0.1mol Cl2,则转移的电子的物质的量为____mol。
答案 : (1)
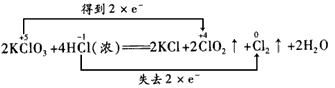
(2)②
(3)0.2
编辑推荐:
下载Word文档

温馨提示:因考试政策、内容不断变化与调整,长理培训网站提供的以上信息仅供参考,如有异议,请考生以权威部门公布的内容为准! (责任编辑:长理培训)






















点击加载更多评论>>